Химические источники тока — это устройства и приборы которые в процессе химической окислительно-восстановительной реакции выделяют напряжение. Также они называются электрохимическими, гальваническими элементами. Основной принцип действия их основан на взаимодействии химических реагентов которые вступая, в реакцию друг с другом вырабатывают электроэнергию, в виде постоянного тока. Этот процесс происходит без механического или теплового воздействия, что является основными факторами играющими превосходящую роль среди других генераторов постоянного напряжения. Химические источники тока, сокращённо ХИТ, уже давно нашли применение не только в быту, но и на производстве.
Немного истории создания ХИТ
Ещё в восемнадцатом веке итальянский учёный Луиджи Гальвани придумал простейший элемент который химическим способом выделял электрический ток. Однако он был не только учёным, но и физиком, врачом, физиологом. Он интересовался и проводил опыты которые были направлены на изучение реакции животных на внешние раздражители. Как и всё гениальное первый химический источник энергии был получен Луиджи абсолютно случайно, во время многочисленных экспериментов над лягушками. После присоединения двух пластин из металла к лягушачьей мышце на лапке, было замечено мускульное сокращение. Гальвани посчитал это нервной реакцией на внешний раздражитель и изложил это в результатах своих исследований, попавших в руки другого великого учёного Алессандро Вольта. Он и выложил свою теорию о возникновении напряжения в результате химической реакции, возникшей между двумя металлическими пластинами в среде мускульной ткани лягушки.
Первый химический источник электрического тока представлял собой емкость с соляным составом, в который было погружено две пластины из разных материалов. Одна из меди, другая из цинка. Именно это устройство в будущем, а конкретнее во второй половине девятнадцатого века, было применено при изобретении и создании марганцево-цинкового элемента внутри которого был тот же солевой электролит.
Передача электричества
Электрический ток – это упорядоченное движение заряженных частиц. Носителями заряда электрического тока в электролитах являются ионы. Они образуются в результате распада (электролитической диссоциации) молекул вещества под действием молекул воды в растворе или при нагревании и образовании расплава.
Расщепление молекул происходит за счёт разрыва полярных ковалентных или ионных связей. Интенсивность диссоциации зависит от температуры и концентрации раствора. Также на степень диссоциации влияет природа электролита. В связи с этим выделяют:
- слабые электролиты, распадающиеся частично или не распадающиеся вообще;
- сильные электролиты, быстро распадающиеся на ионы.
К слабым электролитам относится большинство органических веществ, слабые кислоты, плохо растворимые соли и нерастворимые основания. Сильные кислоты, щёлочи, соли относятся к сильным электролитам.
Рис. 1. Процесс электролитической диссоциации.
Образованные в результате диссоциации ионы делятся на два типа:
- катионы – положительно заряженные частицы;
- анионы – отрицательно заряженные частицы.
Проводником электрического тока в электролитах является электрод. Он может быть анодом или катодом. Анод присоединён к положительному полюсу источника тока, катод – к отрицательному. Анод окисляет вещества, находящиеся в электролите, катод – восстанавливает.
Рис. 2. Электроды.
Если в раствор электролита поместить два электрода – катод и анод – и включить электрический ток, то ионы начнут двигаться под действием электрического поля. Катионы устремятся к катоду, анионы – к аноду. Достигнув электродов, ионы нейтрализуются, превращаются в нейтральные атомы и оседают.
Процесс разложения вещества на составные части, которые оседают на электродах, называется электролизом.
Принцип действия
Источники питания 24 и 12 Вольт
Устройства вырабатывающее электрический ток содержит два электрода, которые помещаются между электролитом. Именно на их границе соприкосновения и появляется небольшой потенциал. Один из них называют катодом, а другой анодом. Все эти элементы вместе образуют электрохимическую систему. Во время возникновения окислительно-восстановительной реакции между электродами один элемент отдаёт мельчайшие частицы электроны другому. Поэтому она и не может происходить вечно, а со временем просто теряются свойства каждого элемента этой цепи. Электроды могут быть представлены в виде пластин или решёток из металла. После погружения их в среду с электролитом меду их выводами возникает разность потенциалов, которая именуется напряжением разомкнутой цепи. Даже при удалении хотя бы одного из электродов с электролита процесс генерации напряжения прекращается.
Состав электрохимических систем
В качестве электролита используются следующие химические вещества:
- Водные растворы на основе щелочей, кислот, солей и т. д.;
- Растворы с ионной проводимостью на неводной основе, которые получены при растворении солей в неорганических или органических растворителях;
- Твердые соединения, содержащие ионную решетку, где один из ионов является подвижным;
- Матричные электролиты. Это особый вид жидких растворов и расплавов, которые находятся в порах твёрдого непроводящего элемента — электроносителя;
- Расплавы солей;
- Ионообменные электролиты с униполярной системой проводимости. Твёрдые тела с фиксированной ионогенной группой одного знака.
Принцип работы
Химический источник, который вырабатывает постоянный ток, имеет определенный принцип работы. Алгоритм выработки электроэнергии посредством протекания химических реакций между некоторыми веществами достаточно прост для понимания, разобраться с этим сможет человек, далекий от химии или физики.
Важно! Из-за использования достаточно агрессивных типов веществ, которые входят в состав таких источников, самостоятельно вскрывать конструкции запрещено. Это может нанести вред здоровью и жизни. Дополнительно требуется определенная утилизация.
Между окислителем и восстановителем (электролитом) протекает окислительно-восстановительная реакция. В результате выделяются электроны, которые начинают последовательно двигаться в определенном направлении. Именно благодаря выделенной в результате химреакции энергии и происходит движение элементарных заряженных частиц.
Так и получается электрический ток, который нужно уметь еще и добыть. Если не создать нужные условия для выхода электронов на внешнюю цепь, то вещество будет выделять только тепло. Чтобы это сделать, нужно подготовить два электрода: анод (где происходит окисление) и катод (восстанавливает вещество).
Вам это будет интересно Для чего нужно выравнивание потенциалов
Принцип устройства химического источника тока
Величина электроэнергии, которая получается в результате протекания окислительно-восстановительной реакции, зависит от таких факторов:
- объем и концентрация электролита;
- материал, из которого изготовлены электроды;
- конструкция внешней электрической цепи.
Есть несколько вариантов наиболее эффективных и применяемых электролитов с определенной концентрацией и массой.
Классификация гальванических элементов и их подбор
Основные понятия о релейной защите
Генераторы электрического тока получающегося во время химической реакции разделяются по:
- Размерам;
- Конструктивным особенностям;
- Способу и реагенту, за счёт которого, и получается электроэнергия.
Все элементы вырабатывающее ток во время химической реакции делятся на:
- Заряжаемые, которые в процессе эксплуатации могут неоднократно заряжаться от источника постоянного тока, они называются аккумуляторами;
- Не заряжаемые, то есть источники одноразового использования которые после завершения химической реакции просто приходят в негодность и должны быть утилизированы. Попросту это гальванический элемент или батарейка.
Для того чтобы подобрать источник электроэнергии, основанный на химической реакции, нужно понимать его характеристики, к которым относятся:
- Напряжение между анодом и катодом при разомкнутой цепи. Этот показатель чаще всего зависит от выбранной электрохимической системы, а также концентрации и вылечены всех составляющих;
- Мощность источника;
- Показатель силы тока;
- Емкость;
- Электротехнические показатели, то есть количество циклов заряда и разряда;
- Диапазон рабочих температур;
- Срок хранения между тем временем как элемент был создан и до начала его эксплуатации;
- Полный срок службы;
- Прочность, то есть защита корпуса от различных механических повреждений и влияний, а также вибраций;
- Положение работы, некоторые из них работают только в горизонтальных положениях;
- Надёжность;
- Простота в эксплуатации и обслуживании. В идеале отсутствие необходимости малейшего вмешательства в работу в течение всего срока эксплуатации.
При выборе нужной батареи или аккумулятора обязательно нужно учесть его электрические номиналы такие как напряжение и ток, а также ёмкость. Именно она является ключевой для сохранения работоспособности, подключаемого к источнику прибора.
упорядоченное (направленное) движение электрически заряженных частиц или заряженных макроскопич. тел. За направление тока принимают направление движения положительно заряженных частиц; если ток создаётся отрицательно заряженными частицами (напр., электронами), то направление тока считают противоположным направлению движения частиц.
Различают Э. т. проводимости, связанный с движением заряженных частиц относительно той или иной среды (т. е. внутри макроскопич. тел), и конвекционный ток —
движение макроскопич. заряженных тел как целого (напр., заряженных капель дождя).
О наличии Э. т. в проводниках можно судить по тем действиям, к-рые он производит: нагреванию проводников, изменению их хим. состава, созданию магнитного поля. Магнитное действие тока проявляется у всех без исключения проводников; в сверхпроводниках
не происходит выделения теплоты, а хим. действие тока наблюдается преимущественно в
электролитах.
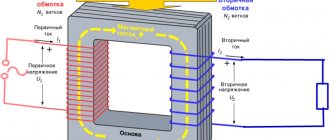
Магнитное поле порождается не только током проводимости или конвекционным током, но и переменным электрическим полем в диэлектриках и вакууме. Величину, пропорциональную скорости изменения электрического поля, во времени, Дж. К.
Максвелл
назвал
током смещения.
Ток смещения входит в
Максвелла уравнения
на равных правах с током, обусловленным движением зарядов. Поэтому полный Э. т., равный сумме тока проводимости и тока смещения, может быть определён как величина, от к-рой зависит интенсивность магнитного поля. Количественно Э. т. характеризуется скалярной величиной —
силой тока I
и векторной величиной —
плотностью электрического тока j.
При равномерном распределении плотности тока по сечению проводника сила тока
I — jS = q0nvS,
где qo — заряд частицы,
п —
концентрация частиц (число частиц в единице объёма),
v —
ср. скорость направленного движения частиц, S — площадь поперечного сечения проводника.
Для возникновения и существования Э. т. необходимо наличие свободных заряженных частиц (т. е. положительно или отрицательно заряженных частиц, не связанных в единую электрически нейтральную систему) и силы, создающей и поддерживающей их упорядоченное движение. Обычно силой, вызывающей такое движение, является сила со стороны электрич. поля внутри проводника, к-рое определяется электрическим напряжением
на концах проводника. Если напряжение не меняется во времени, то в проводнике устанавливается
постоянный ток,
если меняется,-
переменный ток.
Важнейшей характеристикой проводника является зависимость силы тока от напряжения — вольтамперная характеристика.
Она имеет простейший вид для металлич. проводников и электролитов: сила тока прямо пропорциональна напряжению
(Ома закон).
В зависимости от способности веществ проводить Э. т. они делятся на проводники, диэлектрики
и
полупроводники,
В проводниках имеется очень много свободных заряженных частиц, а в диэлектриках — очень мало. Поэтому сила тока в диэлектриках крайне мала даже при больших напряжениях, и они служат хорошими
изоляторами.
Промежуточную группу составляют полупроводники.
В металлах свободными заряженными частицами — носителями тока являются электроны проводимости, концентрация к-рых практически не зависит от темп-ры и составляет 1022-1023см-3.
Их совокупность можно рассматривать как «электронный газ». Электронный газ в металлах находится в состоянии вырождения
,
т. е. в нём отчётливо проявляются квантовые свойства. Квантовая теория металловобъясняет зависимость электрич. сопротивления металлов от темп-ры (линейное увеличение с ростом темп-ры) и прямую пропорциональность между силой тока и напряжением
.
В электролитах Э. т. обусловлен направленным движением положит, и отрицат. ионов. Ионы образуются в электролитах в результате электролитической диссоциации.
С ростом темп-ры число молекул растворённого вещества, распадающихся на ионы, увеличивается и сопротивление электролитов падает. При прохождении тока через электролит ионы подходят к электродам и нейтрализуются. Масса выделившегося на электродах вещества определяется законами электролиза Фарадея.
Газы из нейтральных молекул являются диэлектриками. Э. т. проводят лишь ионизованные газы — плазма.
Носителями тока в плазме служат положит, и отрицат. ионы (как в электролитах) и свободные электроны (как в металлах). Ионы и свободные электроны образуются в газе в результате сильного нагревания или внеш. воздействий (
ультрафиолетового излучения, рентгеновских лучей,
при соударениях быстрых электронов с нейтральными атомами или молекулами и т. д.
).
Э. т. в электровакуумных приборах (электронных лампах, электроннолучевых трубках и т. д.) создаётся потоками электронов, испускаемых нагретым электродом — катодом (см. Термоэлектронная эмиссия).
Электроны ускоряются электрич. полем и достигают другого электрода — анода.
В полупроводниках носителями тока являются электроны и дырки.
Л
ит.: Тамм И. Е., Основы теории электричества, 9 изд., М., 1976, гл. 3, 6; Калашников С. Г., Электричество, 4 изд., М., 1977 (Общий курс физики), гл. 6, 14-16, 18. Г. Я. Мякишев.
По материалам БСЭ.
Современные химические источники тока и их применение
Знакомство с пиковыми и другими зонами тарификации электроэнергии
Современный быт человека тяжело приставить без этих мобильных генераторов энергии, с которыми он сталкивается в течение всей жизни, начиная с детских игрушек и заканчивая, допустим, автомобилем.
Сферы применения различных батареек и аккумуляторов настолько разнообразны что перечислить их очень сложно. Работа любого мобильного телефона, компьютера, ноутбука, часов, пульта дистанционного управления была бы невозможна без этого переносного и очень компактного устройства для создания стабильного электрического заряда. В медицине широко используются источники химической энергии при создании любого аппарата, помогающего человеку полноценно жить. Например, для слуховых аппаратов и электрокардиостимуляторов которые могут работать только от переносных источников напряжения, чтобы не сковывать человека проводами. В производстве применяются целые системы аккумуляторных батарей для обеспечения напряжением цепей отключения и защит в случае пропадания входящего высокого напряжения на подстанциях. И также широко применяется это питание во всех транспортных средствах, военной и космической технике. Одним из видов распространённых батарей являются литиевые источники электрического тока, так как именно этот элемент обладает высоким показателем удельной энергии. Дело в том что только этот химический элемент, оказывается, обладает сильным отрицательным потенциалом среди всех известных и изученных человеком веществ. Литий-ионные батареи выделяются среди всех остальных элементов питания по величине вырабатываемой энергии и низким габаритам, что позволяет применять их в самых компактных и мелких электронных устройствах.
Классификация
Самые распространенные виды — гальванические элементы и аккумуляторы. С ними знаком практически каждый. Но классификация таких приспособлений более широкая и предполагает еще и существование топливных элементов.
Схема классификации источников тока
Гальванические элементы
Гальванический элемент получил свое название в честь ученого Гальвано, который и открыл чудесную возможность получения электрического тока посредством создания простой конструкции из электролита и электродов. Они считаются первыми прототипами современных устройств для получения электроэнергии благодаря химическим реакциям.
Вам это будет интересно Все об электрических токах
Химические источники тока — гальванические элементы и аккумуляторы
Обратите внимание! В настоящее время это приспособление имеет более компактный и безопасный для использования вид, это обычная батарейка. Особенность работы такого устройства заключается в том, что использование его одноразовое. После окончательного разложения электролита на вещества, повторно зарядить их для следующих реакций невозможно.
Электрические аккумуляторы
Электрический аккумулятор — это более универсальный вариант устройства, который можно заряжать несколько раз после потери заряда электролита. Такая особенность объясняется регенерацией веществ, которые образуют электролит.
Устройство аккумулятора
В данном случае зарядка производится от постороннего (внешнего) источника тока. Часто с такой потребностью в восстановлении реагента в аккумуляторах сталкиваются автомобилисты, производя зарядку аккумулятора.
Топливные элементы
Электрохимический топливный элемент является перспективным источником, который достаточно важен для создания комфортных и в некоторых ситуациях жизненно необходимых условий существования.
Тепловой химический источник
Особенность работы такого элемента заключается в следующем. К электродам каждый раз поступает определенная порция электролита, которая после разрядки выводится из конструкции. Например, резервный генератор тока благодаря такому принципу работы может производить электроэнергию в течение 10-15 лет.
Обратите внимание! После истечения срока эксплуатацию можно продлить, если восстановить питание.
Способы утилизации химических источников энергии
Проблема утилизации разных по габаритах химических источников напряжения является экологической проблемой всей планеты. Современные источники содержат в себе до тридцати химических элементов которые могут нанесите ощутимый вред природным ресурсам, поэтому для их утилизации разработаны целые программы и построены специализированные цеха по переработке. Некоторые методы позволяют не только качественно перерабатывать эти вредные вещества, но и возвращать в производство, тем самым защитив окружающую среду. В целях извлечения цветных металлов из батарей и аккумуляторов в настоящий момент разработаны и применены в цивилизованных странах, следящих и заботящихся об окружающей среде, целые пирометаллургические и гидрометаллургические комплексы. Самый же распространённый способ утилизации отработанных химических источников тока является метод, работающий на соединении этих процессов. Главным его достоинством считается высокая степень извлечения с минимальным количеством отходов. Этот метод пирометаллургической, гидрометаллургической и механической переработки включает в себя восемь основных стадий:
- Измельчение;
- Магнитная сепарация;
- Обжиг;
- Дополнительное измельчение;
- Выделение крупных и мелких элементов с помощью грохочения;
- Водное очищение и выщелачивание;
- Сернокислотное выщелачивание;
- Электролиз.
Организация правильного сбора и утилизации ХИТ позволяет максимально уменьшить негативное влияние как на окружающую природу, так и на здоровье самого человека.
Современное применение ХИТ
Источники тока химические в настоящее время применяются в:
- транспортных средствах;
- переносных приборах;
- военной и космической технике;
- научном оборудовании;
- медицине (электрокардиостимуляторы).
Привычные примеры ХИТ в быту:
- батарейки (сухие батареи);
- аккумуляторные батареи переносных бытовых приборов и электроники;
- источники бесперебойного питания;
- автомобильные аккумуляторы.
Особенно широкое применение получили литиевые химические источники тока. Это связано с тем, что литий (Li) обладает самой высокой удельной энергией. Дело в том, что он отличается самым отрицательным электродным потенциалом среди всех прочих металлов. Литий-ионные аккумуляторы (ЛИА) опережают все прочие ХИТ по величинам удельной энергии и рабочего напряжения. Сейчас они постепенно осваивают новую сферу — автомобильный транспорт. В дальнейшем разработки ученых, связанные с усовершенствованием литиевых элементов питания, будут двигаться в направлении сверхтонких конструкций и крупных сверхмощных аккумуляторных батарей.