О галогенах
Из галогенов лишь йод способен обладать признаками свойств, характеризующих металлы. Другие вещества (бром, хлор, астат и фтор) лишены даже косвенных признаков металлов. Когда в 1811 году И. Швейггер, немецкий химик, предложил так называть новое выделенное вещество – хлор, название не прижилось. С 1841 года галогенами стали называть всю группу «солеродов». Так переводится с греческого языка слово галогены.
Можно лучше понять, что такое галоген, если охарактеризовать каждый из элементов, входящих в этот ряд:
- Фтор (F) – содержится в солях горных пород. Преимущественно им насыщены криолит, шпат плавиковый и минералы флюорита;
- Хлор (Cl) – популярный из галогенов, в мире имеется в хлориде натрия, являющегося главным сырьём для хлористых соединений;
- Бром (Br) – элемент, встречающийся в морских водах и солёных водоёмах в качестве соли калия и натрия в сочетании с сульфатами хлора;
- Йод (I) – встречается повсеместно, больше всего йода в морской капусте и водорослях;
- Астат (At) – искусственное вещество в природе не встречается, получают в результате оседания частиц при облучении висмута или тория.
К сведению. Хлорид натрия (NaCl) – один из источников хлора. В быту называется поваренной солью. Присутствует в водной жидкости моря, в естественном состоянии находится как серый минерал – галит.
Кристаллы каменной соли
Галогены
Элементы главной подгруппы VII группы периодической системы – фтор, хлор, бром, йод и астат – называют галогенами, что в переводе с греческого означает «рождающие соли». Действительно, продукты взаимодействия галогенов с металлами представляют собой соли.
Одна из дорог, ведущих в Рим к местам соледобычи, так и называлась – Via Salaria (Соляная дорога). Это древнее название сохранилось и по сей день. Почему же обычной поваренной соли, знакомой каждому с детства, воздают такие почести?
Сегодня она общедоступна, а в древности ее ценили наравне с золотом: римским легионерам порой платили не деньгами, а поваренной солью. Интересно, что английское слово salary – «зарплата» происходит от латинского sal (соль).
Добыча соли из морской воды. Гравюра из книги Г.Агриколы «О горном деле и металлургии». Издание 1557 г. Недалеко от морского берега выкапывают несколько бассейнов, сообщающихся друг с другом и соединенных с морем каналом. Под действием солнечного тепла вода испаряется, а в бассейнах кристаллизуется соль. Её сгребают деревянными граблями и перекладывают в кадки лопатами.
В древности соль добывали из соляных озёр, расположенных неподалеку от устья реки Тибр. Позже ее стали получать из морской воды. Для этого участки суши, затопляемые во время прилива, специально огораживали. По мере испарения воды первой кристаллизовалась поваренная соль. Ее собирали, а остававшийся рассол, содержащий прочие соли, выливали обратно в море.
Соляную кислоту HCl в Средние века называли соляным спиртом. Впервые она упоминается в сочинениях немецкого алхимика Василия Валентина во второй половине XV в. Им описан метод получения соляного спирта сухой перегонкой смеси, состоящей из купороса, квасцов и поваренной соли. Алхимики изучали действие соляного спирта на металлы и оксиды. А вот состав этого вещества долгое время был для учёных загадкой.
Как открывали галогены
Согласно теории кислот, выдвинутой А.Л. Лавуазье, особые их свойства обусловлены присутствием не водорода, а кислорода. Лавуазье высказал гипотезу, что соляная кислота содержит вместе с кислородом (а возможно, и водородом) еще и новый элемент, который он назвал мурием (от лат. muria – «рассол»). Сегодня известно, что этот элемент – хлор.
Свободный хлор (от греч. «хлорос» — «жёлто-зеленый») впервые получен в 1774 г. К.В.Шееле действием соляной кислоты на минерал пиролюзит MnO2:
MnO2 + 4HCl = MnCl2 + Cl2↑ + 2H2O
Но еще долго хлор считали «окисленной соляной кислотой», оксидом элемента мурия, основываясь на свойстве этого газа взаимодействовать с растворами щелочей, подобно кислотным оксидам. В течение многих лет учёные безуспешно пытались восстановить «оксид мурия», пока наконец Г. Дэви в 1810 г. не высказал предположение, что это новое простое вещество. Дэви дал ему название «хлорин» (Chlorine). Оно до сих пор используется в английском языке. Слово «хлор» предложил в 1812 г. Ж.Л. Гей-Люссак. Тогда же была установлена формула соляной кислоты, а кислородную теорию кислот сменила водородная, согласно которой обязательно составной частью является водород.
Флюорит, или плавиковый шпат, CaF2 издревле использовали в качестве флюса – вещества, которое при выплавке металлов добавляют в руду, чтобы понизить ее температуру плавления. Раствор, образующийся при воздействии на флюорит серной кислоты, содержит плавиковую кислоту HF. Уже в XVII в. он служил для вытравливания узоров на стеклянной посуде. В чистом виде эту кислоту в 1771 г. выделил Шееле, а ее состав установил французский ученый Андре Мари Ампер в 1810 г. Он же предложил назвать содержащийся в этой кислоте элемент фтором (от греч. «фторос» — «гибель»).
Минерал флюорит
Заветной мечтой многих поколений химиков было выделить фтор в свободном виде. Одним из первых такую попытку предпринял Дэви, однако проведенный им электролиз плавиковой кислоты не принёс результатов. Скорая смерть помешала учёному продолжить начатые исследования. Химики, посвятившие себя вслед за Дэви проблеме выделения свободного фтора, получили серьёзные отравления, так и не достигнув желаемого, ведь многие из них не представляли, насколько сильным окислителем является этот газ. Профессор Политехнической школы в Париже Эдмонд Фреми даже наблюдал в 1854 – 1856 гг., как образуются отдельные пузырьки фтора при электролизе расплавленного флюорита, но не сумел его собрать. Впервые это удалось в 1886 г. французскому химику Анри Муассану, который в 1887 г. выделил жидкий фтор. Незадолго до смерти Муассану присудили Нобелевскую премию за получение химически чистого фтора.
Бром открыт в 1826 г. французским химиком А.Ж. Баларом. Это была его первая самостоятельная работа, и так случилось, что она увенчалась выдающимся результатом – обнаружением нового химического элемента. Пропуская хлор через соляной рассол, полученный при упаривании морской воды, Балар заметил, что раствор окрашивается в бурый цвет. Современный химик без труда объяснит это явление: хлор вытесняет бром из бромидов, содержащихся в морской воде: 2KBr + Cl2 = 2KCl + Br2.
А. Ж. Балар
По иронии судьбы знаменитый немецкий химик Юстус Либих за несколько лет до Балара фактически держал в руках водный раствор брома, но не обратил на него внимания, приняв за соединение хлора с йодом. Досадуя на свою самонадеянность, Либих впоследствии говорил: «Не Балар открыл бром, а бром открыл Балара».
Комиссия Парижской академии наук рекомендовала назвать новый элемент, исходя из свойств его соединений, аналогично названиям других галогенов. Таким отличительным свойством учёные сочли резкий неприятный запах этого вещества. Название элемента образовано от греческого слова «бромос», что означает «зловоние».
Позднее бром стали получать кипячением подкисленного рассола с пиролюзитом MnO2:
MnO2 + 2NaBr + 2H2SO4 = MnSO4 + Br2 + Na2SO4 + 2H2O.
В 1811 г. французский химик Бернар Куртуа из золы морских водорослей выделил йод (от греч. «иодес» — «фиолетовый», по цвету паров).
Существование самого тяжелого из галогенов – астата было предсказано Д.И. Менделеевым, который назвал его экаиодом, т.е. первым аналогом йода. Однако получен он был лишь в 1940 г. группой американских ученых из Калифорнийского университета. Все изотопы астата радиоактивны и имеют небольшой период полураспада – не более 8,1часа. Отсюда и название элемента, образованное от греческого «астатос» — «неустойчивый».
Общие физические и химические свойства галогенов
Молекулы простых веществ-галогенов при обычных условиях имеют состав Г2, т.е. F2, Cl2, Br2, I2. Все галогены имеют характерный запах, ядовиты.
Сверху вниз в подгруппе с ростом порядкового номера закономерно изменяются физические свойства простых веществ-галогенов: температура кипения и плавления, агрегатное состояние.
Фтор – газ светло – зеленого цвета; хлор – легко сжижающийся газ желто-зеленого цвета; бром – тяжелая жидкость красно-бурого цвета; йод – твердое кристаллическое вещество с металлическим блеском. Растворимость простых веществ-галогенов в воде в подгруппе сверху вниз уменьшается. Фтор активно взаимодействует с водой, хлор – сравнительно мало растворим в воде, еще менее растворимы в воде бром и йод.
Так как у атомов галогенов на внешнем электронном слое имеется один неспаренный электрон, для них характерна валентность I.
Кроме фтора, у атомов всех галогенов в возбужденном состоянии может увеличиваться число неспаренных электронов, а поэтому соответственно числу неспаренных электронов атомы галогенов в соединениях могут проявлять валентность III, V, VII.
Окислительная способность атомов и молекул галогенов сверху вниз в подгруппе уменьшается от фтора к йоду, так как с увеличением радиуса атома способность галогена присоединять электроны уменьшается, т.е. уменьшаются неметаллические свойства галогенов. Фтор – самый сильный окислитель, так как атом фтора имеет наименьший радиус по сравнению с атомами других галогенов.
Окислительную активность галогенов несложно сопоставить, изучив реакции вытеснения одних галогенов другими из водных растворов галогенидов. Наблюдается такая закономерность: галоген с меньшим порядковым номером вытесняет из солей галоген с большим порядковым номером. Например, бром вытесняет йод из йодидов: Br2 + 2KI = I2 + 2KBr, но не реагирует с хлорид-ионами.
Ионы галогенов (кроме F—) способны отдавать электроны, поэтому они являются восстановителями. Восстановительная способность галогенид-ионов увеличивается от хлорид-иона к йодид-иону: Cl— →Br— → I—.
Все галогены легко взаимодействуют с водородом по уравнению: Г2 + Н2 = 2НГ
Галогеноводороды (HF – фтороводород, HCl – хлороводород, HBr – бромоводород, HI – йодоводород) – это газообразные соединения, легко растворяются в воде. Водные растворы галогеноводородов являются кислотами: HF – фтороводородная (плавиковая), HCl – хлороводородная (соляная), HBr – бромоводородная, HI – йодоводородная.
В ряду кислот HF→ HCl→ HBr→ HI происходит усиление кислотных свойств. Это можно объяснить тем, что сверху вниз в подгруппе галогенов с увеличением заряда ядра атома увеличиваются радиусы атомов. Из всех бескислородных кислот йодоводородная кислота является самой сильной.
Известен ряд соединений галогенов с кислородом. Однако все эти соединения неустойчивы, не получаются при непосредственном взаимодействии элементов с кислородом и могут быть получены только косвенным путем. Из кислородсодержащих соединений наиболее устойчивы соли кислородсодержащих кислот. Во всех кислородсодержащих соединениях галогены, кроме фтора, проявляют положительные степени окисления +1, +3, +5 и +7.
В ряду кислородсодержащих кислот HClO→ HClO2→ HClO3→ HClO4 наблюдается усиление кислотных свойств.
Скачать:
Скачать бесплатно реферат на тему: «Галогены» Галогены.docx (213 Загрузок)
Скачать рефераты по другим темам можно здесь
*на изображении записи фотография минерала флюорита
Похожее
Строение атомов и степени окисления
Основные химические источники электроэнергии
Электронная формула наружной орбиты атомов солеродов – ns2np5. При расположении по порядку:
- F — 2s22p5;
- Cl — 3s23p5;
- Br — 4s24p5;
- I — 5s25p5;
- At — 6s26p5.
Атомы галогенов успешно добавляют к 7 своим электронам, имеющимся на крайней оболочке, один чужой недостающий. Потому при взаимодействии обнаруживают степень (-1) окисления. В союзах, где присутствуют элементы, имеющие электроотрицательность выше, только фтор не меняет степени (-1).
Остальные изменяют её на положительную степень: Cl (+1), Br (+3), I (+5), At (+7).
Графическая картинка электронного строения атома бора Br
Значение понятия галогены
Галогены – это элементы из периодической таблицы Менделеева 17 группы, а по устаревшей классификации – 7 главной подгруппы. К галогенам относится всего 5 химических элементов, среди которых фтор, хлор, иод, астат и бром. Все они являются неметаллами. Галогены – очень активные окислители, а на внешнем уровне данные элементы имеют по 7 электронов.
Что такое галогены, почему они получили такое название? Слово «галоген» образовалось от двух греческих слов, которые в совокупности означают «рождение соли». Один из элементов этой группы – хлор, вместе с натрием образует соль.
Распространённость элементов и получение простых веществ
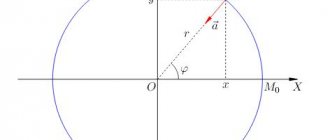
Чем больше величина атомного радиуса, тем меньше наличие солеродов в теле планеты. Величина r – радиуса атома фтора, по сравнению с радиусом атома иода, говорит о том, что фтор более распространён, нежели йод. Астата в коре планеты всего лишь граммы.
Переходное сопротивление
Промышленность производит галоиды (устаревшее название) в больших объёмах. При этом по количеству изготовленной продукции лидирует хлор.
Простые вещества получают при помощи галогенидов, окисляя их. Для этого используется электролитическое окисление. Причём из-за того, что положительные потенциалы у фтора и хлора достаточно высокие, приходится применять сильные окислители.
Важно! Электролиз фтора осложнён невозможностью использования водных растворов. Его потенциал окисления выше, и он может вступать в реакцию с водой, поэтому используют плавиковую кислоту.
Электролиз NaCl с применением анодов из графита позволяет добывать хлор. Катоды при этом могут быть:
- железные;
- жидкие ртутные;
- стальные.
Уравнение, описывающее эту реакцию, имеет вид:
2Cl- —› Cl2 (г.) + 2е-.
Выполняя химическое окисление бромида-иона из морской воды, получают бром.
Так же добывают и йод, используя насыщенные им рассолы. Оба процесса проводят, применяя хлор в виде окислителя. Воздушным потоком, проходящим через раствор, удаляются I2 и Br2.
Производство галогенов, формулы окисления
Характеристика веществ
Узнаем, что такое галогены в химии. Характеристика списка галогенов следующая:
- строение внешнего слоя электронов — nS2nP5,
- по мере роста номера в таблице радиус атома становится больше, электроотрицательность падает, свойства неметалла снижаются,
- являются выраженными окислителями, причем эта способность элементов снижается по мере увеличения массы атома (единственное, с чем не реагирует галоген, — это благородные газы),
- все молекулы содержат 2 атома,
- сила кислот увеличивается по мере роста относительной массы атома.
Периодическая таблица показывает, что чем выше находится элемент, тем сильнее его окислительные способности.
Окислительные свойства атомов
Фтор
При нормальных условиях является бледно-желтым газом. Можно получить путем электролиза КНF2. Реагирует с водой с образованием фтороводорода и кислорода. Реакция водорода и фтора происходит очень активно. Взаимодействует с металлами и неметаллами.
Хлористоводородная кислота является слабой, фтороводород обратимо диссоциирует в воде с выходом ионов Н+ и F-.
Фтороводородная кислота способна растворить стекло:
SiO2 + 4НF → SiF4 + 2Н2О.
Хлор
Является газом зеленоватого цвета с удушающим запахом. Примеры реакций, с помощью которых можно его получить:
- МnO2 + 4НCl → МnСl2 + Сl2+ 2Н2O,
- 2КМnO4 + 16НCl → 2МnСl2 + 5Сl2 + 2КСl + 8Н2O.
Узнаем, каковы химические свойства хлора:
- Взаимодействие с металлами: 2К + Сl2 → 2КСl.
- Реакция с неметаллами: 2Р + 3Сl2 → 2РСlЗ.
- Реакции с щелочами: Сl2 + Сa(ОH)2 → CaОCl2 + H2O.
- Вытеснение йода: Cl2 + 2→ 2 + I2.
Список распространенных кислот:
- хлорноватистая кислота HClO (степень окисления хлора +1),
- хлористая кислота HClO2 (степень окисления +3),
- хлорноватая кислота HClO3 (степень окисления +5),
- хлорная кислота HClO4 (степень окисления +7).
Это интересно! Для чего делают и что это такое гидролиз солей
Бром
Бром представляет собой тяжелую темную жидкость с плохим запахом. Многих интересует, с чем он реагирует. Этот элемент вступает в реакцию с:
- металлами: 2Nа + Вr2 → 2NаВr,
- неметаллами: Н2 + Вr2 → 2НВr,
- водой: Н2 + H2O → НВr + НВrO,
- восстановителями: Вr2 + Н2S → S + 2НВr.
Бромистый водород хорошо реагирует с солями, основаниями, окисями металлов.
Галогены
Йод
Йод — кристаллическое вещество темного фиолетового оттенка. Растворяется в спирте, четыреххлористом углероде. Молекулы взаимодействуют с:
- металлами: К + I → KI,
- водородом: H2 + I2 → 2HI,
- основаниями: 3I2 + 6КOH → 5КI + КIO3 + 3H2O.
Йодистоводородная кислота является сильнейшим восстановителем. При реакции солей с ляписом образуется нерастворимое йодистое серебро. Йодная кислота является очень сильным окислителем (степень окисления йода +7).
Что касается астата, его можно получить только искусственным путем. Восстанавливается с помощью диоксида серы, осаждается сероводородом. Реагирует с йодом и бромом. Растворяется слабой соляной и азотной кислотой.
Физические и химические свойства элемента теннесин изучены мало ввиду малой продолжительности существования его изотопов. Предполагается, что тяжелые радиоактивные элементы могут обладать восстановительной активностью.
Физические свойства галогенов
Электролиз
Это характеристики, описывающие цвет, запах, температуры изменения свойств, а также агрегатное пребывание в нормальных условиях.
Физические свойства простых двухатомных веществ
Внимание! Такие токсичные вещества, как галогены, образовывают взаимные соединения: BrCl, ICl, IBr и иные. Три состояния (твёрдое, жидкое и газообразное) присущи солеродам при комнатной температуре.
Химические элементы
Фтор – элемент с атомным номером 9, обозначается символом F. Элементарный фтор впервые был обнаружен в 1886 г. путем выделения его из плавиковой кислоты. В свободном состоянии фтор существует в виде двухатомной молекулы (F2) и является наиболее распространенным галогеном в земной коре. Фтор – наиболее электроотрицательный элемент в периодической таблице. При комнатной температуре является бледно-жёлтым газом. Фтор также имеет относительно небольшой атомный радиус. Его СО – -1, за исключением элементарного двухатомного состояния, в котором его степень окисления равна нулю. Фтор чрезвычайно химически активен и непосредственно взаимодействует со всеми элементами, кроме гелия (He), неона (Ne) и аргона (Ar). В растворе H2O, плавиковой кислоты (HF) является слабой кислотой. Хотя фтор сильно электроотрицателен, его электроотрицательность не определяет кислотность; HF является слабой кислотой в связи с тем, что ион фтора основной (рН> 7). Кроме того, фтор производит очень мощные окислители. Например, фтор может вступать в реакцию с инертным газом ксеноном и образует сильный окислитель дифторид ксенона (XeF2). У фтора множество применений.
Хлор – элемент с атомным номером 17 и химическим символом Cl. Обнаружен в 1774 г. путём выделения его из соляной кислоты. В своём элементарном состоянии он образует двухатомную молекулу Cl2. Хлор имеет несколько СО: -1, +1, 3, 5 и 7. При комнатной температуре он является светло-зеленым газом. Так как связь, которая образуется между двумя атомами хлора, является слабой, молекула Cl2 обладает очень высокой способностью вступать в соединения. Хлор реагирует с металлами с образованием солей, которые называются хлориды. Ионы хлора являются наиболее распространенными ионами, они содержатся в морской воде. Хлор также имеет два изотопа: 35Cl и 37Cl. Хлорид натрия является наиболее распространенным соединением из всех хлоридов.
Бром – химический элемент с атомным номером 35 и символом Br. Впервые был обнаружен в 1826 г. В элементарной форме бром является двухатомной молекулой Br2. При комнатной температуре представляет собой красновато-коричневую жидкость. Его СО – -1, + 1, 3, 4 и 5. Бром более активен, чем йод, но менее активен, чем хлор. Кроме того, бром имеет два изотопа: 79Вг и 81Вг. Бром встречается в виде солей бромида, растворённых в морской воде. За последние годы производство бромида в мире значительно увеличилось благодаря его доступности и продолжительному времени жизни. Как и другие галогены, бром является окислителем и очень токсичен.
Йод – химический элемент с атомным номером 53 и символом I. Йод имеет степени окисления: -1, +1, +5 и +7. Существует в виде двухатомной молекулы, I2. При комнатной температуре является твёрдым веществом фиолетового цвета. Йод имеет один стабильный изотоп — 127I. Впервые обнаружен в 1811 г. с помощью морских водорослей и серной кислоты. В настоящее время ионы йода, могут быть выделены в морской воде. Несмотря на то что йод не очень хорошо растворим в воде, его растворимость может возрасти при использовании отдельных йодидов. Йод играет важную роль в организме, участвуя в выработке гормонов щитовидной железы.
Астат – радиоактивный элемент с атомным номером 85 и символом At. Его возможные степени окисления: -1, +1, 3, 5 и 7. Единственный галоген, не являющийся двухатомной молекулой. В нормальных условиях является металлическим твёрдым веществом чёрного цвета. Астат является очень редким элементом, поэтому о нём известно немного. Кроме того, астат имеет очень короткий период полураспада, не дольше нескольких часов. Получен в 1940 г. в результате синтеза. Полагают, что астат похож на йод. Отличается металлическими свойствами.
В таблице ниже показано строение атомов галогенов, структура внешнего слоя электронов.
| Галоген | Конфигурация электронов |
| Фтор | 1s2 2s2 2p5 |
| Хлор | 3s2 3p5 |
| Бром | 3d10 4s2 4p5 |
| Иод | 4d10 5s2 5p5 |
| Астат | 4f14 5d10 6s2 6p5 |
Подобное строение внешнего слоя электронов обусловливает то, что физические и химические свойства галогенов похожи. Вместе с тем при сопоставлении этих элементов наблюдаются и различия.
Химические свойства галогенов
Способность вступать в реакцию с разными веществами под воздействием сторонних факторов индивидуальна для каждого из рассматриваемых элементов.
Химические особенности солеродов
При вступлении галогенов в связь с медью (малоактивный металл) получаются галогениды с формулой:
CuHal2, где Hal2 – солероды Br, Cl, F.
Когда галогениды вступают в реакцию с галогенами, то тот солерод, который активнее, вытесняет малоактивный из его же раствора. Хлор, являясь окислителем, вступает во взаимодействие в смесях солей йода и брома. Бром не реагирует на хлориды, но может из иодидов выдавить йод.
При воздействии на органические соединения при хлорировании воды или йодировании соли происходит галогенирование. При этом атом галогена вводится в соединение. Галогенирование может осуществляться замещением, расщеплением или присоединением атома солерода к атомной структуре органических соединений.
Интересно. Йод, имея низкие окислительные способности, не выдавливает из солей галогены. С фтором реакции водных сульфитов вообще не получаются, он вступает в содействие с Н2О.
Что такое галогены
Пожалуй, многих не раз интересовал вопрос, что такое галогены в химии. Это элементы, относящиеся к XVII группе таблицы Менделеева. Раньше их причисляли к главной подгруппе VII группы. К галогенам относят фтор, хлор, бром, йод, астат.
Некоторые химики причисляют к ним искусственно синтезированное вещество теннесин с номером 117. Это пример галогена, который обладает радиоактивностью.
Вещества этой группы причисляют к неметаллам. Они считаются сильнейшими окислителями, причем это химическое свойство галогенов изменяется по мере уменьшения порядкового номера. Наиболее активным окислителем является фтор, который способен взаимодействовать даже с кислородом с образованием фторида. Способны проявлять свойства восстановителя со степенью окисления +7 (высшая). Недаром раньше таблица Менделеева помещала галогены в 7 группу.
В процессе химического взаимодействия с металлами образуют соли (отсюда и название). На внешней оболочке содержится 7 электронов. Атомы присоединяют недостающий электрон и таким образом заполняют ее. Следовательно, степень их окисления равна -1. Однако хлор, бром, йод, астат могут иметь степени окисления 1, 3, 5, 7 со знаком плюс (являясь восстановителем).
В этом кроется ответ на вопрос, с чем взаимодействует галоген. Особенности строения этих веществ таковы, что они реагируют практически со всеми элементами.
Интересно! Название «фтор» происходит от греческого «разрушение». Это сильнейший окислитель, который взаимодействует почти с любыми веществами. Атомы фтора не реагируют с неоном, гелием и аргоном и некоторыми фторидами.
Применение галогенов и их соединений
Использование солеродов находит широкое применение в жизни человека. Быт, медицина, химическая промышленность, военное производство – далеко не все области использования солеродов.
По каждому элементу можно рассмотреть следующие моменты:
- F – значимая часть состава фторополимеров, имеющих высокую химическую, коррозионную и термическую стойкости. Фторсодержащие хлорфторуглероды раньше использовались в хладагентах и в аэрозолях.
- Cl – в натуральном виде газ жёлто-зелёного цвета. Хлор употребляется для обеззараживания скважин, воды для питья и искусственных водоёмов. Наиболее частое применение хлора в быту – отбеливание вещей и очищение загрязнённых поверхностей сантехники. Соляная (муриевая) кислота также содержит хлор.
- Br – негорючее вещество, применяется для тушения огня в огнетушителях. Применим бром и в медицине, в качестве успокоительных препаратов и мегалитических средств. В военных целях входит в состав химии отравляющих веществ.
- I – применяется в виде антисептика, является необходимым элементом в организме человека для работы щитовидной железы.
- At – применения не находит ввиду своей сильной радиоактивности.
Спектр применения галогенов
Добавленный в баллон лампы накаливания газ галоген позволяет повысить температуру встраиваемой нити и качество отдачи света. Пары брома или йода, закачанные в колбу, послужили созданию галогенных ламп и светильников.
Важно! У таких источников света реже сгорают спирали, лампы имеют компактные размеры и могут питаться как переменным, так и постоянным напряжением.
Галогеновый свет используется в лампах автомобильных фар, причём конструкция позволяет выполнять установку, как галогенных ламп накаливания в фару, так и обычных. В соревнованиях светодиодного источника в фаре или галогенового пока лидирует последний.
Галогенные соединения и их роль в организме человека
В человеческом организме в разных процентных содержаниях присутствуют соединения солеродов. Превышение концентраций, как и их уменьшение, существенно влияет на состояние организма.
Биологическая миссия галогенов
Токсичность галогенов
Галогены в опасной концентрации и соединениях действуют на человека следующим образом:
- Хлор имеет 2 класс опасности. Концентрация в атмосфере от 1*10-4% уже вызывает раздражение слизистой, доза 0,01% приводит к острому отравлению и остановке дыхания. Это сильный канцероген, вызывающий туберкулёз и способствующий образованию злокачественных опухолей;
- Фтор в соединении фторида натрия – приводит к смерти, попадая внутрь через органы дыхания или пищеварения. Смертельная концентрация – 4-9 г. Первичные симптомы – слюнотечение, рвотные позывы. Вторичные признаки отравления – поражения нервной и сердечно-сосудистой систем.
- Бром вызывает спазмы и удушье при дыхании уже при концентрации 1*10-3 в объёме воздуха. Токсичная доза – 3 г., смертельная – от 34 г., при попадании внутрь человека.
- Йод, при случайном попадании в организм в количестве 3 г. и более, поражает почки и сердечно-сосудистую систему, блокирует рецепторы щитовидной железы.
Применение галогенов и галогенидов в промышленности и в быту приносит больше пользы, чем вреда. Знание допустимых значений концентрации и правил пользования продуктами, в которых применяются солероды, позволяет пользоваться только их положительными качествами.